En los 35 primeros años del pasado siglo, la física nuclear sufrió una completa metamorfosis. A decir verdad, la física nuclear aparece con el modelo atómico de Rutherford. Hasta entonces se pensaba que los átomos eran como un pastel de frambuesas: la masa del pastel eran los protones y los electrones estaban allí incrustados, siendo las frambuesas. Las cargas positivas de los protones se compensaba con las negativas de los electrones dando un ente sin carga total. De repente, este tipo no tubo otra cosa que hacer, y puso una delgada lamina de oro y le empezó a tirar peñazos, no con piedras sino con protones. Aunque trabajaba en la Universidad de Cambridge, este experimento lo hizo en la mejor universidad del mundo, la Universidad de Manchester. Sorpresa la suya cuando vio que solo una pequeña parte del haz de protones golpeaba con algo en su trayectoria, la gran mayoría atravesaba la lamina de como pedro por su casa. Así Rutherford propone un modelo en el que el átomo consistía en un núcleo central muy pequeño pero muy pesado, los protones, y los electrones giraban alrededor suyo, prácticamente sin carga, pero dotando al átomo de tamaño. Todo lo que ves a tu alrededor esta hueco, lo que no ves, también. Este modelo se propone en 1911, y podemos decir que es el principio de la Física nuclear. Conceptualmente, es un avance tremendo hacía entender que las cosas del mundo atómico nada tienen que ver con las cosas que vemos a nuestro alrededor.
| Modelo del pastel |
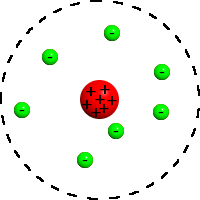 |
| Modelo de Rutherford |
Muchos pasos se van dando en esta joven parte de la física hasta que en 1932, un tal Chadwick descubre el neutrón. El neutrón tienen una importancia vital en nuestra historia, por lo que merece la pena dedicarle un parrafillo. Pensad, en lo alucinante que debería de ser para esta gente el pensar que 30 ó 40 cargas positivas estuvieran junticas, junticas, junticas. Por aquel entonces el electromagnetismo era una rama bastante madura, y todo el mundo sabe que las cosas de igual signo se repelen. ¿Cómo es posible que todos esos protones allí dentro estuvieran como sardinas en lata? ¿Qué extrañas fuerzas pueden hacer que los protones se atraigan? En 1920, Rutherford propone que debía haber algo allí dentro que no dejase escapar a los protones, pero no es hasta doce años después, 1932, cuando este inglés descubre formalmente al nuevo invitado. Así los nucleos pasan a estar formados por protones y neutrones.
La importancia del neutrón es que permite explicar un misterio importante: átomos con las mismas propiedades químicas puedan tener diferente masa. De esta forma, las propiedades químicas de un átomo vienen dadas por el número de protones de su núcleo, mientras que la suma de protones y neutrones determina su masa. Los electrones son tan ligeros que nos podemos olvidar de ellos. Esto era de vital importancia para el proyecto, porque las reacciones químicas eran las mismas para todos los átomos con el mismo número de protones, para una reacción nuclear el número de neutrones se convertía en el factor clave. Expliquemos esto detenidamente:
- Los neutrones son el pegamento nuclear. Pero para pegar 2 protones necesitas solo 2 neutrones, como en el diagrama de arriba, y para pegar los 92 protones del núcleo de uranio, no se necesitan 92 neutrones, sino que se necesitan muchos más. Para unir un núcleo de uranio se necesitan entre 140 y 146 neutrones. Si para un químico, el número de neutrones es un pequeño detalle sin importancia. Desde un punto de vista de un físico nuclear, el numero de protones+neutrones, que como hemos dicho, determina su masa y se llama número másico, se convierte en la principal característica, así en adelante, cuando me oigas decir Uranio-235, o simplemente, U-235, que sepas que me estoy refiriendo no solo a átomos con 92 protones, sino que además, tienen exactamente 143 neutrones en su nucleo. A cada uno de esta clase de átomos de uranio, U-235 y U-238 son los más famosos pero hay otros, se les llama isótopos del uranio.
- Si queremos hacer una bombica, lo primero es determinar que isotopo de que elemento puede tener una reacción nuclear en cadena. El comité encargado de esto, liderado por un tal Arthur Compton, propuso dos candidatos, U-235 y Plutonio-239 (Pu-239). El primer gran problema hacia la fabricación de la bomba era tener unos unos cuantos kilillos de U-235 o Pu-239. Por desgracia, ambos, no se vendían en los supermercados, sino que hay que hay que partir del uranio de las minas para obtenerlo. Cada uno tenía una cosa buena, el U-235, esta en la naturaleza, no hay que generarlo, pero se encuentra junto con su hermano, el U-238, Un kilo de uranio, recién sacado de la mina, tiene 99.3 Kg del hermano aburrido, el U-238, y solamente 0.7Kg del hermano jugueton, el U-235. Hasta entonces, nadie había separado dos isotopos en un proceso industrial, recordar que no se sabía lo que era un isótopo hasta unos pocos años antes. Por otra parte, el Pu-239 se separa mejor del U-238, porque tienen diferentes propiedades químicas, pero el Pu-239 hay que producirlo. Nos tenemos que construir una central nuclear y convertir el U-238 en Pu-239. ¿Cual de los dos escogieron? Escogieron los dos. Con dinero ilimitado y con prisas, elegir un único método era demasiado arriesgado.
Para acabar esta entrada, todo el follón que hay con Irán y su programa nuclear es porque esta separando U-238 de U-235, ellos dicen que para producir energía, pero tener en la despensa un par de kilillos de U-235 en la despensa, te hace ser más respetado.
Me tienes enganchado, a ver como termina esta temporada y si das un avance de la segunda.
ResponderEliminarCreo que el final ya lo sabes, no? Pero quizá algo podamos aprender.
ResponderEliminarLa literatura que estoy usando es:
[1] Manhattan Project: The Untold Story of the Making of the Atomic Bomb.
[2] The German atomic bomb : the history of nuclear research in Nazi Germany.
¿La bomba atómica de Germán? jajaja.
ResponderEliminarTe lo estás currando brutal. La historia es que yo creo que llego a leerlo todo cuando está todo dicho...
PD: Sí, lo comento todo cual tertuliano de programa de sobremesa... jajaja